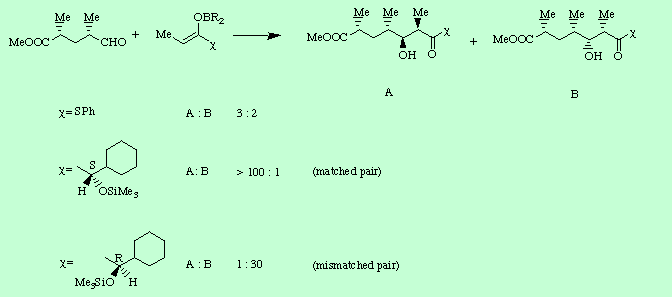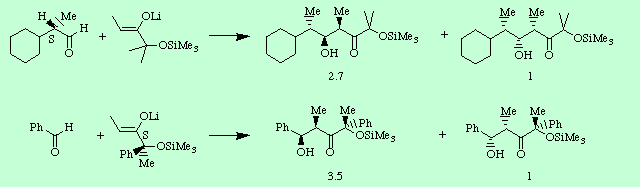
Por una parte se evaluaron las preferencias faciales de las dos reacciones indicadas a continuación, donde uno de los componentes es quiral y otro aquiral. En el primer caso se utilizó un aldehído quiral, de configuración S, frente a un enolato aquiral obteniendose una mezcla de diastereoisómeros en relación 2.7 a 1. En el segundo caso benzaldehído, un aldehído aquiral con caras enantiotópicas, frente a un enolato quiral proporcionando la mezcla representada en relación 3.5 a 1.

Si se observa la configuración relativa de los carbonos 2 y 3 de los cuatro productos se aprecia una relación sin, como cabría esperar de la geometría cis de los enolatos. Pero además de ser sin, los dos productos mayoritarios poseen los grupos hidroxilo y metilo hacia nosotros, mientras que en los minoritarios dichos grupos se alejan. Esto parece indicar que los dos reactivos quirales por separado tienen tendencia a la producción de diastereoselectividad facial en el mismo sentido. Efectivamente, si se hacen reaccionar el aldehído y el enolato quirales la diastereoselección se potencia notablemente, ahora hasta una relación de 8 a 1 en favor del diastereoisómero que guarda la misma relación en sus carbonos 2 y 3 que los mayoritarios en las reacciones anteriores. Sin embargo, esta diastereoselectividad facial disminuye e incluso se invierte si se enfrenta el mismo aldehído que antes con el enolato enantiómero, es decir ahora el R.
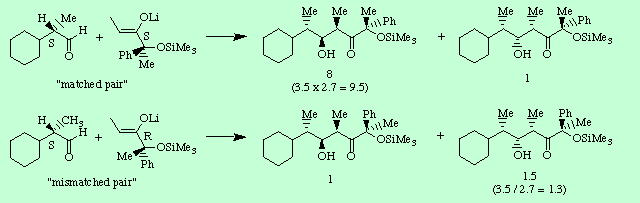
Los dos sustratos quirales que dirigen la inducción en la misma dirección (de ahí el nombre de doble inducción asimétrica) fueron llamados por Masamune como "matched pair", que se podría traducir como par igualado o que combina, mientras que los otros dos los denominó como "mismatched pair" o par que no combina. Además Masamune pronosticó que el grado de diastereoselectividad en una doble inducción asimétrica es aproximadamente igual al producto de las diastereoselectividades faciales de las reacciones patrón para el par combinante y al cociente para el par no combinante.
En este sentido hay que decir que los enolatos de boro, por regla general, muestran una eficacia mayor que los correspondientes de litio en experiencias de doble inducción asimétrica, como se pone de manifiesto en el siguiente caso donde la elección adecuada del par que combina en la misma dirección o "matched pair" lleva a la formación de la mezcla de diastereoisómeros representada en relación 100 a 1. La diastereoselectividad disminuye considerablemente y además se invierte cuando se utiliza el par no combinante.