

Es conocido que un carbono trigonal con tres sustituyentes distintos presenta dos caras enantiotópicas, Re y Si. La adición de un reactivo de forma preferencial por una de ellas dará lugar a una reacción enantioselectiva.

Algunos de los ejemplos más representativos de estos procesos son reacciones de adición nucleófila a cetonas no simétricas, como por ejemplo la reducción de la acetofenona por un agente de transferencia de hidruro. Así, en este caso y para indicar la topicidad absoluta de la reacción se hablará de adición Re de hidruro para dar el alcohol de configuración S o de adición Si para dar el enantiómero.
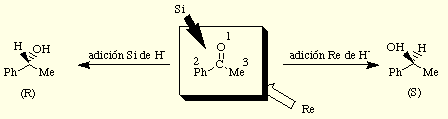
Por otra parte, el sistema de nomenclatura l (like)/u (unlike) introducido por Prelog para describir la configuración relativa de dos estereocentros en diastereoisómeros puede utilizarse también para especificar la topicidad relativa de las reacciones diastereoselectivas[1]. El sistema consiste en comparar las especificaciones R o S de un estereocentro y Re o Si de una unidad proquiral (ya sea ésta una cara o un ligando). De esta forma las combinaciones (R, Re), (S, Si), (Re, Re), y (Si, Si) se denotan como lk (like), mientras que las (R, Si), (S, Re), (Re, Si) y (Si, Re) como ul (unlike).

Por ejemplo, en el siguiente [[alpha]]-amino-ß-cetoácido quiral, en el cual el centro asimétrico posee configuración S, hay dos caras diastereotópicas definidas por el plano que contiene a los grupos unidos al carbono carbonílico, la cara Re que es la que vemos nosotros y la Si que queda por detrás. Si ahora se combinan estas asignaciones, resulta el descriptor lk , que contiene la combinación de centro quiral S y lado Si de la unidad proquiral y ul para la cara que determina la combinación S, Re. Así, la reducción por adición ul de hidruro da el producto de configuración relativa l , mientras que la adición lk conduce al producto u . Como se puede apreciar, y al igual que ocurría en el caso anterior, la topicidad relativa o absoluta de una reacción no está directamente relacionada con la configuración relativa o absoluta de los productos.
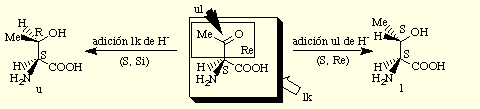
Para reacciones donde se forman dos nuevos estereocentros simultaneamente, como por ejemplo el caso de la reacción del benzaldehído con el enolato del propionato de etilo, se asignan las caras Re y Si de cada uno de los sustratos proquirales y la topicidad relativa de los cuatro posibles modos de reacción se especifica como lk o ul por comparación de las denotaciones Re o Si de cada una de las caras que intervienen en el proceso. Así, por ejemplo la reacción entre la cara Si del benzaldehído y la Re del enolato se denota como ul para dar el producto de configuración relativa u .
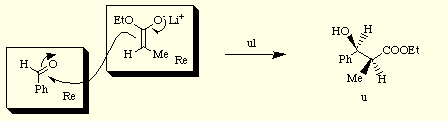
A la vista de estos ejemplos de procesos diastereoselectivos, es decir que transcurren a través de estados de transición con diferentes energías, y donde la formación de uno de ellos se encontrará favorecida sobre la del otro, puede surgir la duda de si se puede predecir cúal es el camino de reacción más favorecido y por tanto si se puede predecir la configuración de los nuevos centros creados. La contestación a esta pregunta es afirmativa para algunos procesos en los que una recopilación de datos experimentales, así como estudios teóricos han permitido la propuesta de algunos modelos que explican y posibilitan la predicción de configuraciones de futuros estereocentros, a partir de unidades proquirales. A continuación se discuten algunos de esos modelos.