
2. En segundo lugar se han clasificado aquellos
métodos en los que se utilizan materiales de partida quirales y
además ópticamente activos, obtenidos de fuentes naturales y
sobre los que se llevan a cabo transformaciones de grupos funcionales presentes
en la molécula hasta llegar al material deseado, pero sin alterar
ninguna de las unidades estereogénicas iniciales. Este tipo de
materiales de partida fueron denominados por Hanessian como quirones (que es la
contracción inglesa de sintón quiral)[1]. Actualmente y proporcionados por la
naturaleza se dispone de una amplia gama de este tipo de compuestos derivados
de aminoácidos, aminoalcoholes, hidroxiácidos, alcaloides,
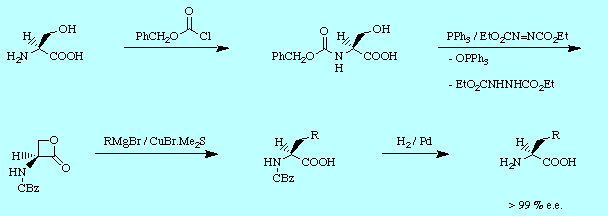
terpenos o azúcares. Con ellos se pueden obtener, como en el siguiente
ejemplo[2], aminoácidos no naturales
(dependiendo del resto R) a partir de otros que sí lo son como la
(S)-serina. La secuencia de reacciones seguida en este caso supone la
protección del grupo amino seguida de una esterificación
intramolecular tipo Mitsunobu, para dar una ß-lactona que sufre una
apertura SN2 con una variedad de reactivos de Grignard, en presencia de sales
de cobre(I). La desprotección del grupo amino conduce a la
obtención de aminoácidos no naturales en un 99% de exceso
enantiomérico. Como se puede apreciar sustrato y producto mantienen la
misma disposición espacial en torno al centro asimétrico y se han
producido interconversiones de grupos funcionales en otros puntos de la
molécula.
 >
>




